Biên bản lựa chọn thuốc đối chứng dùng cho tương đương sinh học
Bạn đang xem tài liệu "Biên bản lựa chọn thuốc đối chứng dùng cho tương đương sinh học", để tải tài liệu gốc về máy hãy click vào nút Download ở trên
Tóm tắt nội dung tài liệu: Biên bản lựa chọn thuốc đối chứng dùng cho tương đương sinh học
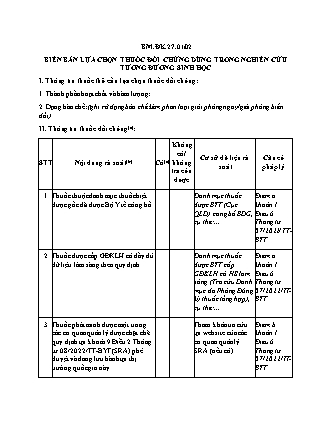
BM.ĐK.27.01/02 BIÊN BẢN LỰA CHỌN THUỐC ĐỐI CHỨNG DÙNG TRONG NGHIÊN CỨU TƯƠNG ĐƯƠNG SINH HỌC I. Thông tin thuốc thử cần lựa chọn thuốc đối chứng: 1. Thành phần hoạt chất và hàm lượng: 2. Dạng bào chế: (ghi rõ dạng bào chế kèm phân loại giải phóng ngay/giải phóng biến đổi) II. Thông tin thuốc đối chứng(a): Không có/ Cơ sở dữ liệu rà Căn cứ STT Nội dung rà soát (b) Có(c) không soát pháp lý tra cứu được 1 Thuốc thuộc danh mục thuốc biệt Danh mục thuốc Điểm a dược gốc đã được Bộ Y tế công bố được BYT (Cục khoản 1 QLD) công bố BDG, Điều 6 cụ thể:... Thông tư 07/2022/ TT- BYT 2 Thuốc được cấp GĐKLH có đầy đủ Danh mục thuốc Điểm a dữ liệu lâm sàng theo quy định được BYT cấp khoản 1 GĐKLH có HS lâm Điều 6 sàng (Tra cứu Danh Thông tư mục do Phòng Đăng 07/2022/TT- ký thuốc tổng hợp), BYT cụ thể:... 3 Thuốc phát minh được một trong Tham khảo tra cứu Điểm b các cơ quan quản lý dược chặt chẽ tại website của các khoản 1 quy định tại khoản 9 Điều 2 Thông cơ quan quản lý Điều 6 tư 08/2022/TT-BYT (SRA) phê SRA (nếu có) Thông tư duyệt và đang lưu hành tại thị 07/2022/TT- trường quốc gia này BYT 4 Thuốc được một trong các cơ quan - Tham khảo tra cứu Điểm c quản lý dược chặt chẽ quy định tại tại website của các khoản 1 khoản 9 Điều 2 Thông tư cơ quan quản lý Điều 6 08/2022/TT-BYT (SRA) phê duyệt SRA (nếu có) Thông tư và đang lưu hành tại thị trường 07/2022/TT- - Tra cứu dịch vụ quốc gia này (Ưu tiên lựa chọn BYT công dữ liệu cấp thuốc có GĐKLH còn hiệu lực tại GĐKLH tại Việt VN) Nam 5 Thuốc đã được tiền thẩm định Điểm c (prequalified) bởi Tổ chức Y tế thế int/pqweb/medicines khoản 1 giới (Ưu tiên lựa chọn thuốc thuốc /finished- Điều 6 có GĐKLH còn hiệu lực tại VN) pharmaceutical- Thông tư products/prequalified07/2022/TT- BYT Ghi chú: (a) : Căn cứ thành phần hoạt chất, dạng bào chế của thuốc thử, lựa chọn thuốc đối chứng theo quy định tại khoản 2 Điều 6 Thông tư 07. (b) : Thứ tự ưu tiên sẽ áp dụng từ tiêu chí 1 đến tiêu chí 5. Nếu có 1 tiêu chí đáp ứng sẽ không cần rà soát các tiêu chí còn lại. (c) Nếu có ghi rõ thông tin thuốc tra cứu được bao gồm (tên thuốc, hoạt chất, hàm lượng, dạng bào chế, cơ sở sản xuất, nước sản xuất, nước cấp phép lưu hành) Kết luận: Thuốc:........................ (SĐK:........................ ), hoạt chất:........................ hàm lượng:............... , dạng bào chế: , cơ sở sản xuất: ......................nước sản xuất: ...................., nước cấp phép lưu hành: .................. đáp ứng tiêu chí số thứ tự được lựa chọn làm thuốc đối chứng trong nghiên cứu tương đương sinh học của thuốc generic chứa hoạt chất: . , hàm lượng: .. , dạng bào chế: ................. Ngày rà soát Chuyên viên đầu mối/Chuyên gia thẩm định Chữ ký III. Xử lý của Phòng Đăng ký thuốc: 1. Chuyên viên phụ trách (trường hợp thuốc đối chứng đã được cấp GĐKLH tại Việt Nam): - Hiệu lực GĐKLH thuốc đối chứng được lựa chọn: .................................................... - Thông tin thuốc đối chứng đúng với thông tin đã được phê duyệt trong hồ sơ đăng ký thuốc □ - Ý kiến khác □ Ghi rõ ý kiến khác: ......................................................................................................... Ngày rà soát: Chữ ký: 2. Lãnh đạo Phòng kết luận: Trình Hội đồng công bố thuốc đối chứng □ Ý kiến khác □ Ghi rõ ý kiến khác: .......................................................................................................... Ngày rà soát: Chữ ký:
File đính kèm:
 bien_ban_lua_chon_thuoc_doi_chung_dung_cho_tuong_duong_sinh.docx
bien_ban_lua_chon_thuoc_doi_chung_dung_cho_tuong_duong_sinh.docx

