Biên bản thẩm định Pháp chế - Quyết định 242/QĐ-QLD
Bạn đang xem tài liệu "Biên bản thẩm định Pháp chế - Quyết định 242/QĐ-QLD", để tải tài liệu gốc về máy hãy click vào nút Download ở trên
Tóm tắt nội dung tài liệu: Biên bản thẩm định Pháp chế - Quyết định 242/QĐ-QLD
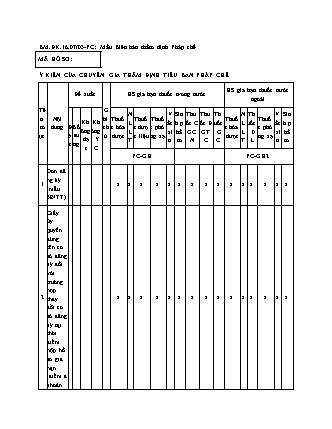
BM.ĐK.16.07/03-PC: Mẫu Biên bản thẩm định Pháp chế MÃ HỒ SƠ: Ý KIẾN CỦA CHUYÊN GIA THẨM ĐỊNH TIỂU BAN PHÁP CHẾ HS gia hạn thuốc nước Đề xuất HS gia hạn thuốc trong nước ngoài Tê G N V Sin Thu Thu Th N Th V Sin n Nội hi Thuố Thuố Thuố Thuố Thuố Kh Kh L ắc h p ốc C ốc Đ uốc L uốc ắc h p m dung ĐBổ ch c hóa c dượ c phó c hóa c phó ôngông L xi hẩ GC GT G L D xi hẩ ục ạ su ú dược c liệu ng xạ dược ng xạ đạ Y T n m N C C T L n m t ng t C PC-GH PC-GH2 Đơn đă ng ký 1 x x x x x x x x x x x x x x x (mẫu 5B/TT) Giấy ủy quyền đứng tên cơ sở đăng ký đối với trường hợp 2 thay x x x x x x x x x x x x x x x đổi cơ sở đăng ký tại thời điểm nộp hồ sơ gia hạn (điểm a khoản 6 Điều 22) Giấy ủ y quyền ký tên trên hồ 3 sơ đăng x x x x x x x x x x x x x x x ký (điểm b khoản 6 Điều 22) Giấy chứng nhận đủ điều kiện kinh doanh dược (đ 4 ối với x x x x x x x x x x x x x x x cơ sở đăng ký của Việt Nam) ( khoản 7 Điều 22) Giấy tờ pháp lý do cơ 5 quan x x x x x x x x x x x x x x x quản lý nhà nước có thẩm quyền nước ngoài cấp (đố i với cơ sở đăng ký nước ngoài) (khoản 9 Điều 22) Giấy phép thành lập văn phòng đại diện tại Việt 6 Nam (đ x x x x x x x x x x x x x x x ối với cơ sở đăng ký nước ngoài) (khoản 8 Điều 22) CPP (khoản 7 x x x x x x 4 Điều 22) Cơ quan 7.1 cấp CPP Nội dung theo mẫu khuyến cáo của WHO được công 7.2bố trên x x x x x x trang thông tin điện tử của WHO (https:// www.w ho.int) Chữ ký , tên người ký, ngày 7.3 x x x x x x cấp, dấu của cơ quan cấp CPP Hiệu lực CP 7.4P (Ghi x x x x x x rõ hiệu lực) Nội 7.5dung x x x x x x xác nhận việc cấp phép và lưu hành thuốc, nguyên liệu làm thuốc trên CPP Product license Holder/ Marketi ng authori 7.6zation x x x x x x holder ( nếu có, ghi rõ tên, địa chỉ, vai trò) Nội dung thẩm định CPP/gi ấy tờ 8 pháp lý x x x x x x cấp bởi cơ quan quản lý quy định tại khoản 9 Điều 2 Thông tư 08/2 022/TT - BYT (n ếu có) (điểm c khoản 4 Điều 22) Ghi chú: Hệ thống lặp lại các yêu cầu đối với CPP từ mục 8.1 đến 8.6 Giấy chứng nhận nguyên liệu làm thuốc được 9 phép x x x x x x sản xuất hoặc lưu hành ở nước sản xuất đối với hồ sơ gia hạn nguyên liệu làm thuốc sản xuất tại nước ngoài (khoản 17 Điều 23) Báo cáo lưu hành thuốc, nguyên liệu làm thuốc 10 x x x x x x x x x x x x x x x theo Mẫu 8/TT ( Ghi rõ đã lưu hành tại VN chưa) Bản sao giấy 11 đăng x x x x x x x x x x x x x x x ký lưu hành thuốc, nguyên liệu làm thuốc tại Việt Nam hoặc bản sao Quyết định cấp GĐKL H trong trường hợp không có MA Các tài liệu liên quan theo quy định tại Phụ lục II T hông tư số 08/2 12 022/TT x x x x x x x x x x x x x x x - BYT tr ong trường hợp thuốc có thay đổi về hồ sơ hành chính tại thời điểm gia hạn (không bao gồm thay đổi mẫu nhãn thuốc và tờ hướng dẫn sử dụng) Nội dung khác (g 13 x x x x x x x x x x x x x x x hi rõ nếu có): Ngày thẩm định Tên chuyên gia Chữ ký Đề xuất của tiểu ban Đạt □ Bổ sung □ Không đạt □ Ý kiến khác □ Nguồn: Quyết định 242/QĐ-QLD năm 2023
File đính kèm:
 bien_ban_tham_dinh_phap_che_quyet_dinh_242qd_qld.docx
bien_ban_tham_dinh_phap_che_quyet_dinh_242qd_qld.docx

